原始生殖细胞(PGC)是在胚胎阶段的生殖系前体,其正常发育对于维持人类生殖健康至关重要。人类在PGC发育机制上与小鼠等模式生物存在差异,由于人类早期胚胎样本获取的伦理限制,目前关于人类PGC的发育调控机制研究进展较慢。
2024年11月19日,Journal of Genetics and Genomics在线发表浙江大学爱丁堡大学联合学院陈迪研究员团队题为“Integrated analysis and systematic characterization of the regulatory network for human germline development”的研究论文。该研究构建了一个全面的人类原始生殖细胞数据库hPGCdb,包含RNA-seq、ATAC-seq、ChIP-seq、scRNA-seq等多组学高通量数据,基于体内与体外不同发育阶段的数据整合性分析,揭示了调控PGC发育的关键转录因子和调控网络,并进行有效性验证,为解析人类生殖系相关疾病靶点提供新思路。

该研究整合了人类PGC相关的大量多组学数据,覆盖了体内和体外、从胚胎干细胞到PGC发育的不同阶段,建立人类PGC数据库(hPGCdb),提供在线分析和可视化平台(http://43.131.248.15:6882)。通过对上述数据的深度整合性分析,该研究成功解析了控制人类生殖细胞命运的潜在关键转录因子和调控网络。研究者通过敲降与敲除实验,验证了潜在的关键基因在生殖细胞发育中的重要作用。此外,进一步解析了原始生殖细胞与其周围体细胞的互相作用网络,确认了SDC2配体和LAMA4受体在PGC发育中的重要作用。最后,该研究发现并验证了体细胞来源的NOTCH2信号推动生殖细胞在体内的进一步分化。
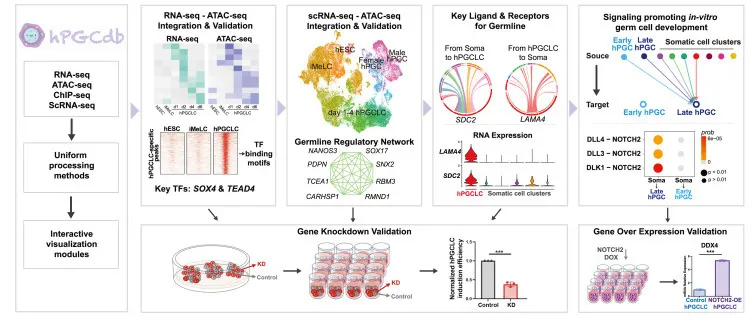
研究整体设计:hPGCdb构建、整合性分析和实验验证
综上所述,该研究不仅加深了我们对PGC生物学的理解,还为相关生殖障碍的诊断和治疗提供了可能的分子靶点。此外,该研究通过CRISPR技术验证了某些关键因子(例如SOX4和TEAD4)在PGC发育中的作用,为未来生殖医学的发展提供了新思路。
浙江大学爱丁堡大学联合学院古雅诗博士为该论文第一作者。浙江大学爱丁堡大学联合学院陈迪研究员、波士顿大学侯磊研究员、爱丁堡大学Robert Young研究员和南方医科大学卫焱星教授为共同通讯作者。相关工作得到国家自然科学基金项目和浙江省自然科学基金项目等项目资助。
原文链接:https://www.sciencedirect.com/science/article/pii/S1673852724003060







